研究成果 東京大学・冨田太一郎 平成21年9月8日
細胞内のストレス応答シグナルを可視化した
冨田太一郎、武川陸寛、Pauline O’Grady、*斎藤春雄 (東京大学・医科学研究所・分子細胞情報分野)*:corresponding author
Molecular and Cellular Biology 29: 6117-6127, 2009
動物の体を構成する個々の細胞はさまざまな環境条件(ストレス)に常にさらされています。例えば、体の表面では紫外線や浸透圧、熱などに曝されます。体内でも、血管や筋肉の細胞には強い圧力がかかったり、場合によっては病原菌や重金属などが侵入してくることもあります。しかし、動物の体を構成する個々の細胞はそのストレスの種類に応じて特定の遺伝子を活性化させたり、細胞の形や性質を変化させたり、また、自ら細胞死を起こすなどして、うまくその個体の生存を維持しています。 しかし、細胞はどのようなしくみで浸透圧や紫外線などの「ストレス」を感じとっているのでしょうか?この問いに答えるために、私たちは先端的な光化学の手法を駆使して、生きた動物細胞内で生じる化学反応をリアルタイムに観察する新規の実験系をつくりました。これによって、細胞内のどこからストレス応答のシグナルが開始されるのかを解明し、未知のストレスセンサーを同定しようという戦略です。我々が注目したのはストレス応答MAPキナーゼとよばれる分子です。これは酵母から線虫、ネズミやヒトに至るまで真核生物に高度に保存されているストレス応答の要の分子ですが、この分子が細胞のどこから活性化されるかを調べました。特に、紫外線については、これまで、核内のDNAの損傷を引き起こすことでストレス応答シグナルを発生させるといわれていました。しかし、実際に観察してみると、紫外線のときのシグナルは核からではなく、細胞質から発生していました。一方で、DNA損傷を起こす抗がん剤のシグナルは予想通り核内から発生しました。百聞は一見にしかずという言葉もありますが、我々の実験結果から、細胞質に未知の紫外線受容のしくみが存在することを容易に見てとることができます。 このストレス応答シグナルの可視化技術は細胞レベルにとどまらず、分子から動物個体のイメージングにまで広く応用可能です。ストレス応答シグナルの異常は神経の異常やがん、あるいは免疫疾患を起こすことがわかってきており、今後個体レベルでストレス応答シグナルを観察することによって、生物学的にも医学的にも重要な知見が得られると期待されます。
クリックで大きい画像へ
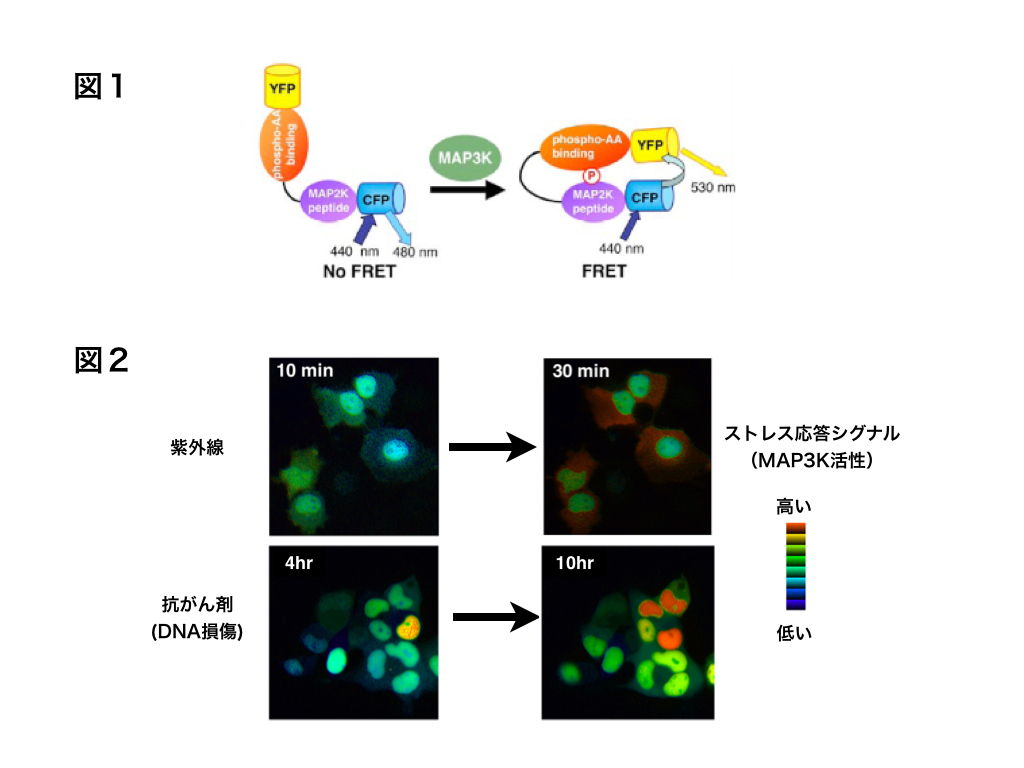
図1:ストレス応答可視化蛍光プローブの模式図。ストレス応答キナーゼ(MAP3K)活性化によりプローブがリン酸化を受けると、プローブの構造変化が生じる。その結果、プローブ両端の蛍光タンパク質分子間の蛍光共鳴エネルギー移動 (FRET) の割合が変化する。従って、ストレス応答キナーゼ活性化により、みかけの黄色蛍光の割合が増える。 図2:細胞のストレス応答シグナル活性化のイメージングの結果。紫外線で刺激した場合には細胞質でシグナルが活性化(赤)した。一方、DNA損傷を引き起こす抗がん剤の場合には、核内からシグナルが活性化する様子が観察された。紫外線とDNA損傷とではシグナル活性化の場所や活性化に要する時間が大きく異なっていた。(図中数字は刺激開始からの時間。)